Les DM de classe I ne sont pas censés présenter de risques importants, l’obtention du marquage CE est beaucoup plus simple que pour les DM de classes supérieures: c’est uniquement le fabricant qui a la responsabilité du marquage CE, il n’y a donc pas de recours à un organisme notifié. Consultez notre page Liens utiles pour connaître les organismes notifiés suivant le RDM.
Ces changements constituent une évolution importante et ils auront un impact sur tous les acteurs du secteur (fabricants, organismes notifiés, etc). Les dispositifs médicaux de classe sont ceux ayant un faible risque, tels que les produits externes de soutien aux patients. Dispositif médical : marquage CE Modalités de mise sur le marché - Les grands principes du marquage CE. En France, l’autorité compétente est l’ANSM.
Il peut y avoir plusieurs organismes notifiés par pays. A ce jour, le seul organisme notifié français pour les dispositifs médicaux est le GMED. Changements de classification. Cas des IVD et des dispositifs médicaux de classe I 1. Cas des dispositifs médicaux destinés aux investigations cliniques et des IVD Instauré dans le cadre de la législation d’harmonisation technique européenne, le marquage CE est un marquage réglementaire qui confère à un certain nombre de dispositifs médicaux le droit de libre circulation sur l’ensemble du territoire de l’Union Européenne.
Voici les étapes majeures à suivre pour l’apposition du marquage CE : 1. Vérification de la conformité selon les Directives sur les dispositifs médicaux. Présentation du guide La réglementation 2. Selon la classe du dispositif et la procédure de marquage CE choisie, tout ou partie d’un système de management de la qualité est exigé par la directive européenne.
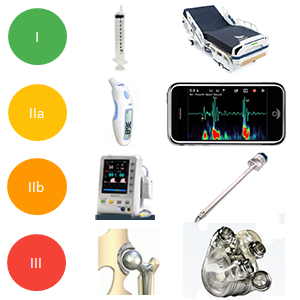
La classe d’un dispositif médical doit être déterminée par son fabricant en suivant un ensemble de règles de classification. Etablissement d’un système de surveillance a posteriori, c’est-à-dire après la mise sur le marché du DM. Détermination du procédé de certification selon la classe.
Pour les DM de classeil s’agit d’une auto-certification par le fabricant qui lui permet d’apposer le marquage CE sur son dispositif. Si un litige survient entre l’organisme notifié et le fabricant sur la classification du DM, il revient à l’autorité compétente de trancher. Dans le cas des DM de classe I, l’autorité compétente peut prendre une décision de police sanitaire pour non-conformité du DM à la réglementation.

Comme pour tous les dispositifs médicaux, un dispositif médical combiné doit obtenir un marquage CE afin de pouvoir être commercialisé en Europe, et dans les pays tiers reconnaissant le marquage CE (Suisse, Turquie, Norvège, …). Il est apposé par le fabricant après obtention d’un certificat de conformité auprès d’un organisme.
Sa tâche principale consiste à certifier la conformité des dispositifs médicaux par rapport aux normes qui régissent le marquage CE. La démonstration du respect de ces normes passe par une procédure de certification qui, en fonction de la classe du dispositif, est réalisée soit par un organisme notifié (classe IIa, IIb et III) soit par un processus d’auto-certification pour les dispositifs les moins dangereux (classe I). Le certificat de conformité délivré par un organisme.

BSI est un fournisseur mondial de services pour les entreprises de dispositifs médicaux dans le monde entier. Nom : GROUPE DIDACTIC : 1. Son « marquage CE » est un passeport communautaire obligatoire pour tous les Dispositifs Médicaux (DM) mis sur le marché de l’Union Européenne. Le Marquage CE est la déclaration du fabricant que son dispositif médical répond aux exigences réglementaires appropriées.
Dispositifs médicaux : thermomètre, pansements, lunettes de vue, dispositif intra-utérin, pacemaker. Pour tout savoir sur les dispositifs médicaux ! III, c’est-à-dire les dispositifs médicaux avec le niveau de risque le plus élevé.
Exemples de dispositifs médicaux implantables actifs : les pacemakers, les défibrillateurs, les implants cochléaires. Avant le toutes les entreprises médicales devront se conformer à celle-ci. Pour circuler en toute liberté dans l’Espace Economique Européen (EEE), les dispositifs médicaux doivent obligatoirement porter la mention marquage CE.
DEKRA Certification, acteur incontournable du secteur médical, vous accompagne dans vos démarche de valorisation de la qualité et de la sécurité de vos produits médicaux. Cela dicte les activités requises pour démontrer la conformité. Formation dispositifs médicaux : comprendre la directive et maîtriser la procédure des marquages CE. Marquage CE des dispositifs médicaux : éléments à fournir lors de l’évaluation de dossier technique.
Le programme Jeudi octobre - 14h30. ADRESSE : Gravotech Marking.
Aucun commentaire:
Enregistrer un commentaire
Remarque : Seul un membre de ce blog est autorisé à enregistrer un commentaire.